#147 - Etilenoglicol na Cerveja
Índice do blog
O objetivo desta postagem é mostrar um método para detectar etilenoglicol na cerveja.
Escrito e desenvolvido por Léo Corradini
O etilenoglicol (1) pode ser usado como aditivo na água usada na refrigeração nas fábricas de cerveja.
Ele abaixa o ponto de congelamento da água, tornando o processo mais eficiente.
Teoria do ensaio:
O reagente clássico para os glicóis é o íon periodato.
O íon periodato reage com o glicol produzindo o íon iodato e formaldeído.
Então, podemos reagir a amostra com o periodato e em seguida podemos facilmente detectar o íon iodato.
O íon iodato reage com o íon iodeto, em meio ácido, produzindo iodo livre que pode ser facilmente detectado pelo amido.
Porém, essa via tem um problema, uma pequena quantidade de iodato que possa vir no periodato dará um falso positivo no ensaio.
Assim, decidi detectar o outro produto da reação, ou seja, o formaldeído.
O formaldeído pode ser evidenciado usando a floroglucina.
A floroglucina reage com o formaldeído em meio alcalino produzindo uma cor avermelhada com intensidade proporcional a quantidade presente.
Reagentes usados no ensaio:
- Solução de periodato de potássio, 100mg de KIO4 em 30mL de água destilada.
- Solução de hidróxido de potássio, um grama de KOH em 30mL de água destilada.
- Solução de floroglucina, 300mg de C6H3(OH)3 em 30mL de água destilada.
- Etilenoglicol - aditivo para radiador
A concentração do aditivo é tipicamente 50%.

Esse aditivo tem um corante fluorescente que ajuda na pesquisa de vazamentos no circuito de refrigeração do motor, basta usar uma lâmpada ultravioleta.
Quantidade de reagentes usados nos ensaios:
Na placa de toque misturei:
- Seis gotas de cada amostra.
- Mais quatro gotas de solução de periodato
- Mais duas gotas de solução de hidróxido
- Mais quatro gotas de solução de Floroglucina.
Teste de sensibilidade do método:
O teste de sensibilidade consistiu em seis ensaios com as seguintes concentrações:
- Somente água destilada
- Uma gota de etilenoglicol 50% em 10 mL de água.
- Uma gota de etilenoglicol 50% em 20 mL de água.
- Uma gota de etilenoglicol 50% em 30 mL de água.
O teste mostra boa sensibilidade, mesmo com a maior diluição, ainda podemos distinguir claramente a cor avermelhada.
Primeiro ensaio, com duas amostras de cerveja:
Nessa primeira abordagem, temos seis ensaios comparativos.
Dois ensaios com água destilada e quatro ensaios com duas amostras de cerveja.
Sendo um ensaio com a amostra pura e outro ensaio com a adição de etilenoglicol.
Para simular uma amostra contaminada, coloquei duas gotas de etilenoglicol em 10mL da água e também em 10mL das duas amostras de cerveja.
Resultados:
As duas amostras de água mostraram a maior variação de cor.
A amostra de água pura mostra um tom azulado e a amostra de água com etilenoglicol a cor avermelhada como esperado.
Já as duas amostras de cerveja mostram tons de vermelho nos quatro ensaios.
Um pouco mais forte nas amostras aditivadas, como esperado.
Ensaio de oito amostras de cerveja:
Cada mL tem 20 gotas, portanto são duas gotas de contaminante para 200 gotas de cerveja.
Como a concentração do etilenoglicol usado é 50% temos que cerveja contaminada ficou com aproximadamente 0,5% de etilenoglicol.
Embaralhei os dois frascos com a amostras, de forma que eu não sabia mais qual cerveja estava contaminada.
Uma segunda pessoa pingou seis gotas das duas amostras de cerveja de forma aleatória na placa de toque.
Assim, temos nas placas de toque, seis amostras contaminadas e seis amostras normais distribuídas de forma randômica.
Em seguida, coloquei os reagentes detectores de etilenoglicol nas doze amostras.
Depois que alguns segundos, podemos ver que seis amostras apresentam um vermelho mais pronunciado que correspondem às amostras que estão contaminadas.
A segunda pessoa participante do ensaio confirmou que as amostras que deram positivo (mais avermelhadas) correspondem a mesma amostra.
Ele pode ser útil sim, como podemos ver no segundo e terceiro ensaios, ele foi capaz de detectar a adição de etilenoglicol.
Certamente, uma cerveja que tenha níveis perigosos de qualquer glicol será prontamente evidenciada por este ensaio.
Um experimento simples para demonstrar o perigo da ingestão do etilenoglicol.
O etilenoglicol é metabolizado em nosso organismo em ácido oxálico, este reage com os íons de cálcio produzindo oxalato de cálcio que é muito insolúvel.
Assim, o etilenoglicol, além de roubar o essencial cálcio do organismo, entope os rins com os finos cristais de oxalato de cálcio.
O tubo da esquerda contém 6 mL de água e 6 gotas da solução de cloreto de cálcio, o tubo da direita contém, além do cálcio, 6 gotas da solução de ácido oxálico.
Uma opção interessante para o etilenoglicol é o propilenoglicol, este é metabolizado em ácido lático muito menos tóxico.
(1) Também são usados o dietilenoglicol e o propilenoglicol, todos são anticongelantes.
O teste é sensível aos três tipos.
O objetivo desta postagem é mostrar um método para detectar etilenoglicol na cerveja.
Escrito e desenvolvido por Léo Corradini
O etilenoglicol (1) pode ser usado como aditivo na água usada na refrigeração nas fábricas de cerveja.
Ele abaixa o ponto de congelamento da água, tornando o processo mais eficiente.
Teoria do ensaio:
O reagente clássico para os glicóis é o íon periodato.
O íon periodato reage com o glicol produzindo o íon iodato e formaldeído.
Então, podemos reagir a amostra com o periodato e em seguida podemos facilmente detectar o íon iodato.
O íon iodato reage com o íon iodeto, em meio ácido, produzindo iodo livre que pode ser facilmente detectado pelo amido.
Porém, essa via tem um problema, uma pequena quantidade de iodato que possa vir no periodato dará um falso positivo no ensaio.
Assim, decidi detectar o outro produto da reação, ou seja, o formaldeído.
O formaldeído pode ser evidenciado usando a floroglucina.
A floroglucina reage com o formaldeído em meio alcalino produzindo uma cor avermelhada com intensidade proporcional a quantidade presente.
Reagentes usados no ensaio:
- Solução de periodato de potássio, 100mg de KIO4 em 30mL de água destilada.
- Solução de hidróxido de potássio, um grama de KOH em 30mL de água destilada.
- Solução de floroglucina, 300mg de C6H3(OH)3 em 30mL de água destilada.
- Etilenoglicol - aditivo para radiador
A concentração do aditivo é tipicamente 50%.

Esse aditivo tem um corante fluorescente que ajuda na pesquisa de vazamentos no circuito de refrigeração do motor, basta usar uma lâmpada ultravioleta.
Quantidade de reagentes usados nos ensaios:
Na placa de toque misturei:
- Seis gotas de cada amostra.
- Mais quatro gotas de solução de periodato
- Mais duas gotas de solução de hidróxido
- Mais quatro gotas de solução de Floroglucina.
A mudança de cor ocorre em ~15 segundos.
Teste de sensibilidade do método:
O teste de sensibilidade consistiu em seis ensaios com as seguintes concentrações:
- Somente água destilada
- Uma gota de etilenoglicol 50% em 10 mL de água.
- Uma gota de etilenoglicol 50% em 20 mL de água.
- Uma gota de etilenoglicol 50% em 30 mL de água.
- Uma gota de etilenoglicol 50% em 40 mL de água.
- Uma gota de etilenoglicol 50% em 50 mL de água.O teste mostra boa sensibilidade, mesmo com a maior diluição, ainda podemos distinguir claramente a cor avermelhada.
Primeiro ensaio, com duas amostras de cerveja:
Nessa primeira abordagem, temos seis ensaios comparativos.
Dois ensaios com água destilada e quatro ensaios com duas amostras de cerveja.
Sendo um ensaio com a amostra pura e outro ensaio com a adição de etilenoglicol.
Para simular uma amostra contaminada, coloquei duas gotas de etilenoglicol em 10mL da água e também em 10mL das duas amostras de cerveja.
As duas amostras de água mostraram a maior variação de cor.
A amostra de água pura mostra um tom azulado e a amostra de água com etilenoglicol a cor avermelhada como esperado.
Já as duas amostras de cerveja mostram tons de vermelho nos quatro ensaios.
Um pouco mais forte nas amostras aditivadas, como esperado.
Ensaio de oito amostras de cerveja:
Conclusão:
Todas as amostras mostraram alguma alteração na cor.
Sendo que a amostra #5 apresentou um avermelhado mais intenso.
Possíveis causas:
- Adição de etilenoglicol no processo.
- A fermentação gera algum glicol.
- Algum componente desconhecido da cerveja causa alteração da cor neste teste.
Neste terceiro ensaio, bolei um pequeno protocolo de análise:
Usei duas amostras de 10mL da mesma cerveja e adicionei duas gotas de etilenoglicol 50% em uma delas.
Cada mL tem 20 gotas, portanto são duas gotas de contaminante para 200 gotas de cerveja.
Como a concentração do etilenoglicol usado é 50% temos que cerveja contaminada ficou com aproximadamente 0,5% de etilenoglicol.
Embaralhei os dois frascos com a amostras, de forma que eu não sabia mais qual cerveja estava contaminada.
Uma segunda pessoa pingou seis gotas das duas amostras de cerveja de forma aleatória na placa de toque.
Assim, temos nas placas de toque, seis amostras contaminadas e seis amostras normais distribuídas de forma randômica.
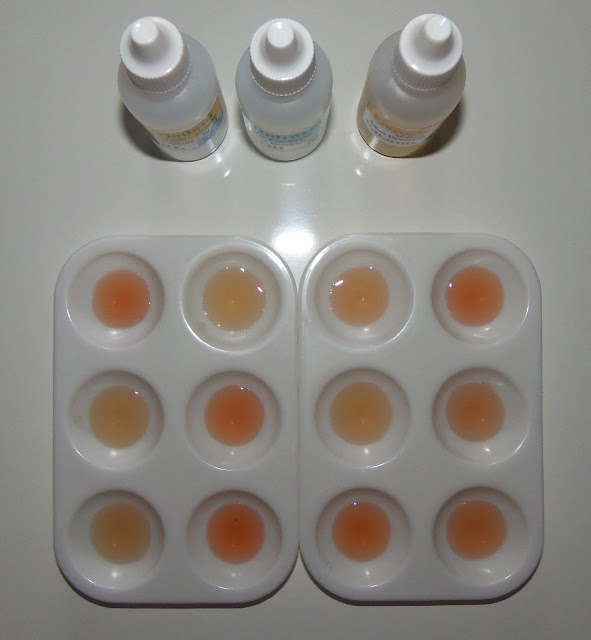
Em seguida, coloquei os reagentes detectores de etilenoglicol nas doze amostras.
Depois que alguns segundos, podemos ver que seis amostras apresentam um vermelho mais pronunciado que correspondem às amostras que estão contaminadas.
A segunda pessoa participante do ensaio confirmou que as amostras que deram positivo (mais avermelhadas) correspondem a mesma amostra.
Então, esse método é útil ou não ?
Ele pode ser útil sim, como podemos ver no segundo e terceiro ensaios, ele foi capaz de detectar a adição de etilenoglicol.
Certamente, uma cerveja que tenha níveis perigosos de qualquer glicol será prontamente evidenciada por este ensaio.
Um experimento simples para demonstrar o perigo da ingestão do etilenoglicol.
O etilenoglicol é metabolizado em nosso organismo em ácido oxálico, este reage com os íons de cálcio produzindo oxalato de cálcio que é muito insolúvel.
Assim, o etilenoglicol, além de roubar o essencial cálcio do organismo, entope os rins com os finos cristais de oxalato de cálcio.
O tubo da esquerda contém 6 mL de água e 6 gotas da solução de cloreto de cálcio, o tubo da direita contém, além do cálcio, 6 gotas da solução de ácido oxálico.
Uma opção interessante para o etilenoglicol é o propilenoglicol, este é metabolizado em ácido lático muito menos tóxico.
(1) Também são usados o dietilenoglicol e o propilenoglicol, todos são anticongelantes.
O teste é sensível aos três tipos.
















Comentários
Postar um comentário